পদার্থবিদ্যা
আপেক্ষিক তাপ
আপেক্ষিক তাপ হলো কোনো পদার্থের তাপ ধারণ ক্ষমতার পরিমাপ। সহজ ভাষায় বলতে গেলে, একই পরিমাণ তাপ প্রয়োগ করলে কোন পদার্থের তাপমাত্রা কতটুকু বৃদ্ধি পাবে তা নির্দেশ করে আপেক্ষিক তাপ।
আপেক্ষিক তাপের সংজ্ঞা:
- ভরের আপেক্ষিক তাপ: একক ভরের কোনো পদার্থের তাপমাত্রা ১ ডিগ্রি সেলসিয়াস বৃদ্ধি করতে যে পরিমাণ তাপ প্রয়োজন তাকে ঐ পদার্থের ভরের আপেক্ষিক তাপ বলে। ভরের আপেক্ষিক তাপের একক হলো J/kg°C (জুল প্রতি কেজি প্রতি ডিগ্রি সেলসিয়াস)।
- মোলার আপেক্ষিক তাপ: এক মোল কোনো পদার্থের তাপমাত্রা ১ ডিগ্রি সেলসিয়াস বৃদ্ধি করতে যে পরিমাণ তাপ প্রয়োজন তাকে ঐ পদার্থের মোলার আপেক্ষিক তাপ বলে। মোলার আপেক্ষিক তাপের একক হলো J/mol°C (জুল প্রতি মোল প্রতি ডিগ্রি সেলসিয়াস)।
তাপমাত্রা হলো একটা জিনিস ঠান্ডা না গরম তার একটা পরিমাণ!
এটা আমাদের দৈনন্দিন জীবনের অভিজ্ঞতা থেকেই তো বোঝা যায় তাইনা ? আমরা প্রতিদিনের পরিবেশের তাপমাত্রা চ্যাক করি , জ্বর হলে বলি তাপমাত্রা বেড়েছে কিংবা ঠান্ডা লাগলে বলি তাপমাত্রা কমেছে ইত্যাদি ইত্যাদি । অনেকেই আবার তাপ ও তাপমাত্রাকে গুলিয়ে ফেলেন । দুটো বিষয় আসলেই আলাদা ।
চলুন ,এবার একটু অন্যভাবে তাপ ও তাপমাত্রাকে দেখা যাক ।
- শুরুতে তাপ নিয়ে কিছু বলি । তাপ আসলে কী? ছোটবেলায় আমরা পড়েছি তাপ হচ্ছে শক্তি ! ঠিক যেমন বিদ্যুৎ শক্তি, রাসায়নিক শক্তি, শব্দশক্তি ! শক্তির একটা ধর্ম হচ্ছে শক্তি কাজ করতে পারে অর্থাৎ বল প্রয়োগে বস্তুকে বলের দিকে সরাতে পারে! আচ্ছা তা না হয় বুঝলাম , কিন্তু তাপশক্তি তৈরী হয় কীভাবে? আপনি জেনে অবাক হবেন যে, তাপশক্তি আসলে গতিশক্তি ছাড়া কিছুই না ! এ্যা? এটা কীভাবে?
- আমরা যদি কোন বস্তুর অনুগুলোকে জুম করে দেখতে পারতাম অর্থাৎ আনবিক পর্যায়ে দেখতে পারতাম তাহলে দেখতাম সেগুলো ক্রমাগত নিজ নিজ জায়গায় কাপছে! এটাকেই বলে কাইনেটিক থিওরি অব পার্টিকেল !
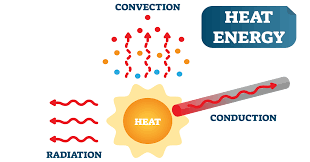
- কাপুনী বাড়তে থাকলে এক পর্যায়ে অনুগুলো নিজেদের আন্তঃআনবিক আকর্ষন বল’কে ছিন্ন করে আলাদা হয়ে যাবে । সেই অনুযায়ীই আমরা পদার্থের কঠিন, তরল ,বায়বীয় বিভিন্ন অবস্থার ব্যাখা দিই আরকী! সম্মিলিত গতিশক্তি যত বাড়ে তাপ তত বাড়ে ! তাই আমরা তাপকে বলেছি গতিশক্তি! এখন তাপমাত্রা তাহলে কী? তাপমাত্রা আসলে এই যে গতিশক্তির কথা বললাম তার একটা গড় পরিমাপ!
নিশ্চয় খেয়াল করেছেন এখন আমরা সত্যিকার তাপমাত্রা বলতে কী বোঝায় সেটা বোঝার চেষ্টা করছি ।
এবার তাহলে একটা উদাহরণ দিয়ে বিষয়টা আরও সহজ করা যাক ।
মনে করুন, এক বিকার জলে একটা গরম আলপিনকে ডুবালাম ।
এটা যেহেতু একটা থট এক্সপেরিমেন্ট আপনি চিন্তা করুনতো, গরম আলপিন কী ঠান্ডা হবে আরও আরও গরম হয়ে উঠবে?
উত্তর নিশ্চয় পেয়ে গেছেন , ঠান্ডা হবে তাইনা? কিন্তু কেন? এক গ্লাস জলে তো তাপ(গতিশক্তি) অনেক বেশি রয়েছে, তার তুলনায় ছোট্ট গরম আলপিনটায় তো তাপ (গতিশক্তি) থাকার কথা খুব কম । তাহলে কেন গরম আলপিনটির অল্প তাপশক্তি চলে গেল বেশি তাপশক্তির বিকারের জলে? ব্যাপারটা কীভাবে ব্যাখা করা যায়? উত্তরটা দেবে তাপমাত্রা
কারন তাপমাত্রা হচ্ছে সেই জিনিস যেটা নির্নয় করে একটা বস্তু অন্য বস্তুর সংস্পর্শে আসলে সেটা কী তাপ দেবে নাকী তাপ নেবে!
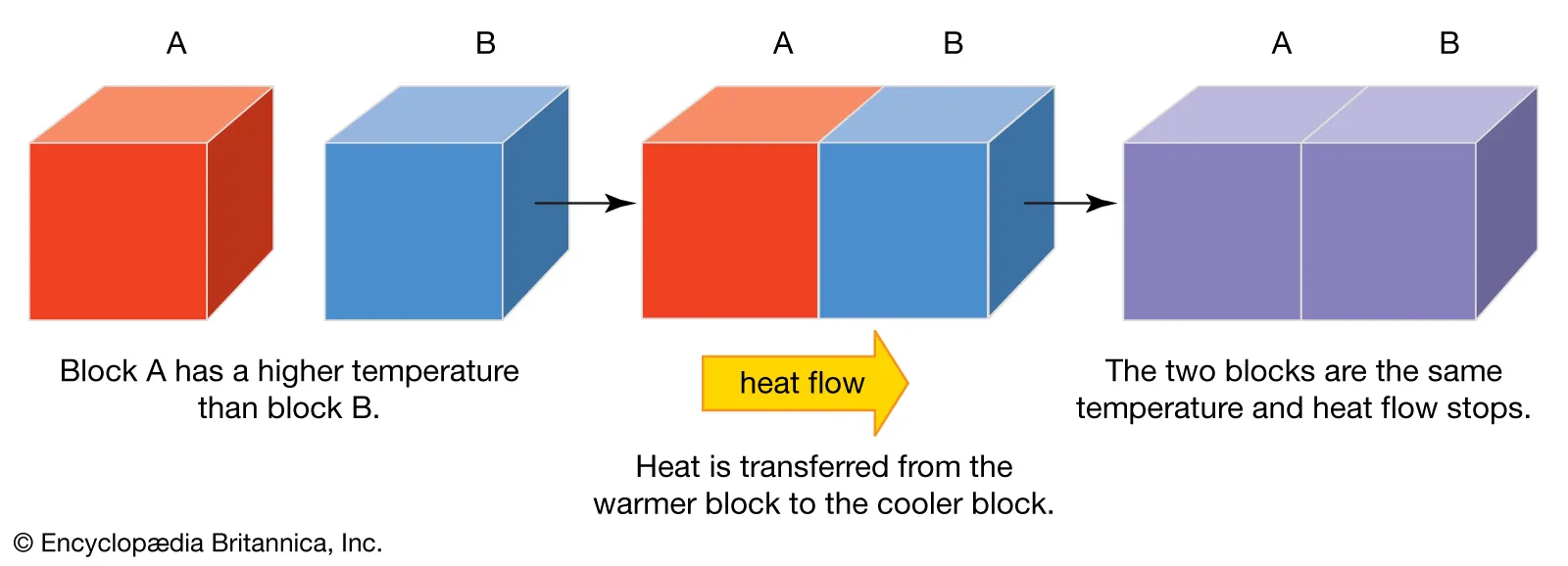
তাপমাত্রা হল একটি পরিমাণ যা গরম এবং ঠান্ডা বা কোন পরমাণু বা অণুর গড় গতিশক্তির পরিমাপ প্রকাশ করে। তাপমাত্রা বা উষ্ণতা হচ্ছে কোনো বস্তু কতটা গরম (উষ্ণ) বা ঠান্ডা (শীতল), তার পরিমাপ এবং তাপশক্তি পরিবহণ দ্বারা সবসময় উষ্ণতর বস্তু থেকে শীতলতর বস্তুতে প্রবাহিত হয়। উষ্ণতা কোনো বস্তুর মোট তাপের পরিমাপ নয়, তাপের “মাত্রা”র’ পরিমাপ। এই মাত্রা বস্তুর কোনো অংশের স্থানীয় তাপজনিত আণবিক চাঞ্চল্যের পরিমাণের উপর নির্ভর করে।তাপমাত্রা হলো তাপের বহিঃপ্রকাশ ।

গ্যাসের ক্ষেত্রে দুটি আপেক্ষিক তাপ
গ্যাসের ক্ষেত্রে উষ্ণতা বৃদ্ধি করলে একই সঙ্গে গ্যাসের আয়তন ও চাপ দুটোই পরিবর্তন হয়।
সেই জন্য একবার গ্যাসের চাপে (P) স্থির রেখে উষ্ণতা বৃদ্ধিতে শুধুই গ্যাসের আয়তন(V) বৃদ্ধি ঘটানো হয় এর থেকে গ্যাসের যে প্রসারণ গুণাঙ্ক পাওয়া যায় তাকে গ্যাসের আয়তন প্রসারণ গুণাঙ্ক বলে এবং Cp প্রকাশ করা হয়।
অপরদিকে একবার গ্যাসের আয়তন (V)স্থির রেখে উষ্ণতা বৃদ্ধিতে শুধুই গ্যাসের চাপের(P) পরিবর্তন ঘটানো হয় এক্ষেত্রে গ্যাসের যে প্রসারণ গুণাঙ্ক পাওয়া যায় তাকে গ্যাসের চাপের প্রসারণ গুণাঙ্ক বলা হয় এবং Cv প্রকাশ করা হয়।
প্রতি ক্ষেত্রে গ্যাসের প্রাথমিক উষ্ণতা 0°c ধরা হয়।
Cp=(Vt-V₀)/t যখন গ্যাসের চাপ P স্থির।
Cv=(Pt-P₀)/t যখন গ্যাসের আয়তন V স্থির।
V₀ ,P₀, t হল যথাক্রমে শূন্য ডিগ্রী সেলসিয়াস তাপমাত্রায় গ্যাসের আয়তন, 0 ডিগ্রি উষ্ণতায় চাপ এবং t হল গ্যাসের তাপমাত্রা বৃদ্ধি
Vt ,Pt হল যথাক্রমে t°cউষ্ণতায় গ্যাসের আয়তন ও চাপ।

